A partir de hoje, um dos medicamentos mais populares no tratamento do diabetes tipo 2 e amplamente conhecido também pelo uso no controle de peso entra em uma nova fase no Brasil.
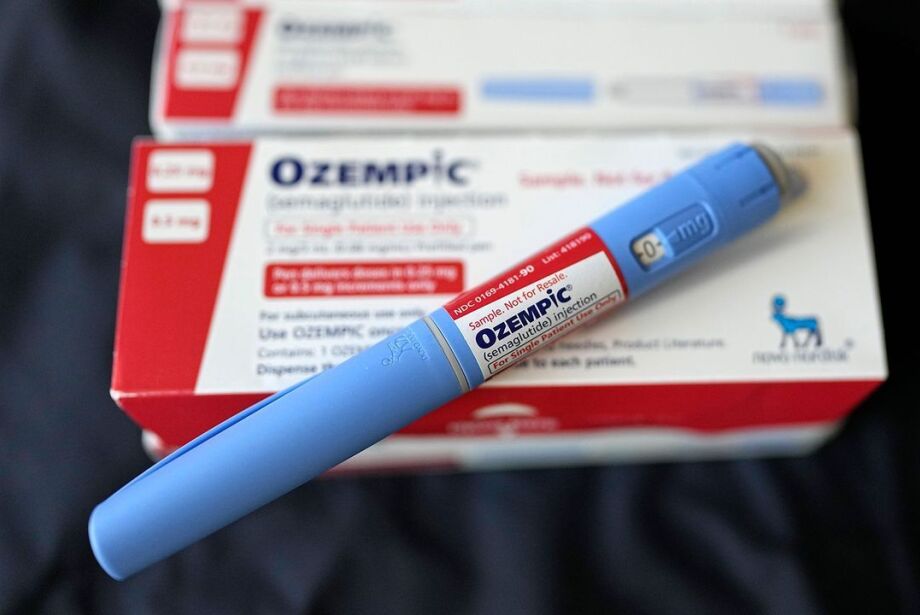
A patente da semaglutida, princípio ativo do Ozempic, chega ao fim após decisão do Superior Tribunal de Justiça (STJ), que optou por não prorrogar a proteção exclusiva da fórmula no País.
Na prática, a medida abre o mercado para a produção de versões genéricas e similares, o que pode impactar diretamente o preço e o acesso ao tratamento.
Até então, a farmacêutica Novo Nordisk detinha exclusividade na fabricação e comercialização da semaglutida. Com o término da patente, outras empresas passam a ter autorização para desenvolver medicamentos com o mesmo princípio ativo, desde que cumpram as exigências regulatórias.
Em 2025, a Anvisa passou a priorizar as análises para liberação das canetas para empresas nacionais. Por isso, o primeiro registro da semaglutida no Brasil pode sair ainda no fim de maio, com as farmacêuticas Àvita Care, EMS e Megalabs à frente na corrida.
A pressa das empresas se dá para garantir a conquista de um mercado que movimentou R$ 10 bilhões com as canetas emagrecedoras no último ano e promete movimentar R$ 15,6 bilhões em 2026.
QUEDA DE PREÇOS
Um dos efeitos mais esperados com a quebra da exclusividade é a redução no preço. Atualmente, a caneta de Ozempic pode custar cerca de R$ 1.000, valor que limita o acesso de muitos pacientes. Especialistas do setor farmacêutico apontam que, com a entrada de novos fabricantes, o preço pode cair entre 30% e 50% ao longo dos próximos anos.
Esse movimento segue uma lógica já observada com outros medicamentos: quanto maior a concorrência, menor tende a ser o custo final para o consumidor.
No entanto, essa redução não deve acontecer de forma imediata ou uniforme. Fatores como escala de produção, logística e estratégia comercial das empresas influenciam diretamente no valor final nas farmácias.
PRODUÇÃO NACIONAL
A expectativa em torno da quebra da patente já mobiliza o setor farmacêutico. Empresas brasileiras e multinacionais estão em uma espécie de “corrida industrial” para lançar suas próprias versões da semaglutida.
Parcerias para produção local também começam a ser estruturadas, o que pode fortalecer a indústria nacional e reduzir a dependência de importações.
Além disso, a produção local tende a facilitar a distribuição do medicamento e, potencialmente, acelerar sua chegada a diferentes regiões do País. Ainda assim, o processo exige investimentos em tecnologia e infraestrutura, especialmente por se tratar de um medicamento biológico complexo.
Por fim, a chegada dos genéricos às farmácias ainda depende da aprovação pela Agência Nacional de Vigilância Sanitária (Anvisa). Atualmente, diversos pedidos de registro de versões da semaglutida estão em fase final de análise.
A agência é responsável por avaliar a segurança, eficácia e qualidade dos medicamentos antes de autorizar sua comercialização. Esse processo pode levar meses, o que significa que os consumidores podem não ver mudanças imediatas nas prateleiras.
No caso de medicamentos biológicos, como a semaglutida, as versões alternativas são conhecidas como biossimilares – produtos altamente semelhantes ao original, mas não idênticos, exigindo estudos mais complexos para comprovação de equivalência.
IMPACTO NO SUS
Outro ponto central da discussão é o impacto da quebra da patente no Sistema Único de Saúde (SUS). Com a tendência de redução de preços, cresce a possibilidade de o SUS incorporar a semaglutida em suas políticas de tratamento.
Hoje, o acesso ao medicamento pelo sistema público é limitado, principalmente em razão do alto custo. Com versões mais baratas disponíveis, o cenário pode mudar, ampliando o tratamento para pacientes com diabetes tipo 2 e, eventualmente, obesidade – duas condições que representam desafios crescentes para a saúde pública no Brasil.
A inclusão no SUS, no entanto, depende de avaliações de custo-benefício e da incorporação oficial por órgãos responsáveis, como a Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec).
Decisão do STJ
Em janeiro, a 4ª Turma do Superior Tribunal de Justiça (STJ) decidiu não prorrogar o prazo de vigência das patentes dos medicamentos Ozempic e Rybelsus, ambos utilizados no tratamento do diabetes tipo 2 e também no controle do peso corporal.
A ação foi movida pela farmacêutica dinamarquesa Novo Nordisk, em conjunto com a Novo Nordisk Farmacêutica do Brasil Ltda., contra o Instituto Nacional da Propriedade Industrial (Inpi).
As empresas alegaram demora na análise dos pedidos de patente e solicitaram o reconhecimento da chamada “mora administrativa”, com a consequente extensão do prazo de exclusividade.
O pedido, no entanto, já havia sido negado nas instâncias anteriores. Os tribunais entenderam que, após o julgamento da ação direta de inconstitucionalidade (ADI) nº 5.529 pelo Supremo Tribunal Federal (STF), ficou estabelecido que a validade das patentes de invenção no Brasil é de 20 anos, contados a partir do depósito do pedido no Inpi, sem possibilidade de prorrogação judicial em razão de atrasos administrativos.
Ao analisar o caso, o Tribunal Regional Federal da 1ª Região (TRF1) destacou que a Constituição Federal prevê a exploração exclusiva de invenções por prazo determinado.
Segundo a Corte, eventuais usos indevidos por terceiros podem gerar direito à indenização desde a data do depósito do pedido, o que não altera o limite temporal da patente.
No recurso ao STJ, as farmacêuticas voltaram a argumentar que houve demora excessiva por parte do Inpi na tramitação dos processos e pediram a extensão das patentes por mais 12 anos.
As empresas também defenderam que o direito à indenização não substitui o período de exclusividade garantido pela patente e que o Estado deve reparar os prejuízos causados pela demora administrativa.
Apesar dos argumentos, a 4ª Turma do STJ manteve o entendimento das instâncias anteriores e rejeitou o pedido de prorrogação das patentes.

 O anuário estatístico do turismo de Bonito – ano-Base 2025 mostra índices expressivos no município e na região da Serra da Bodoquena. Os dados, divulgados pelo observatório do turismo e eventos de Bonito (oteb), indicam que foram recebidos 293.712 visitantes no ano que passou, número que mantém o destino em patamar elevado de fluxo turístico, após a forte recuperação registrada no período pós-pandemia. Mostram também a alta procura pelos atrativos naturais: foram registradas 880.669 visitações, consolidando a localidade como um dos principais destinos de ecoturismo do País. Em 2025, o aeroporto regional da cidade contabilizou 36.388 desembarques, o maior volume da série histórica desde a retomada das operações regulares. O número representa cerca de 12,39% dos turistas que chegaram ao destino utilizando o modal aéreo. Na hotelaria, a taxa média de ocupação ficou em 53%, mantendo estabilidade em relação ao ano anterior e demonstrando a consolidação do setor após o período de retomada do turismo.
O anuário estatístico do turismo de Bonito – ano-Base 2025 mostra índices expressivos no município e na região da Serra da Bodoquena. Os dados, divulgados pelo observatório do turismo e eventos de Bonito (oteb), indicam que foram recebidos 293.712 visitantes no ano que passou, número que mantém o destino em patamar elevado de fluxo turístico, após a forte recuperação registrada no período pós-pandemia. Mostram também a alta procura pelos atrativos naturais: foram registradas 880.669 visitações, consolidando a localidade como um dos principais destinos de ecoturismo do País. Em 2025, o aeroporto regional da cidade contabilizou 36.388 desembarques, o maior volume da série histórica desde a retomada das operações regulares. O número representa cerca de 12,39% dos turistas que chegaram ao destino utilizando o modal aéreo. Na hotelaria, a taxa média de ocupação ficou em 53%, mantendo estabilidade em relação ao ano anterior e demonstrando a consolidação do setor após o período de retomada do turismo. Rosana Razuk e Dr. Claudio Razuk
Rosana Razuk e Dr. Claudio Razuk Dra. Beatriz Graf
Dra. Beatriz Graf






